检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
/ 老版新葡萄8883官网 / 学术科研
cGAS是胞质内的双链DNA或Mn2+ 受体,也是一个二核苷酸环化酶,被DNA和/或Mn2+ 激活后利用细胞质中的ATP和GTP合成第二信使2’3’-cGAMP ,后者进一步激活STING,最终诱导I-型干扰素及抗病毒/肿瘤免疫反应;Mn2+ 单独激活的cGAS则以一种更高效的路径合成2’3’-cGAMP。胞质中任何来源的DNA都能激活cGAS,细胞受到的各种压力胁迫,如氧化、代谢及DNA受损等都可导致细胞器Mn2+ 的释放。因此,cGAS不仅是DNA感受器,也是细胞压力和基因组不稳定的传感器,在自身免疫病、细胞损伤/衰老及肿瘤免疫监视中起重要作用。Mn2+ 单独使用或Mn2+ 和PD-1抗体联合使用的“锰免疗法”都可显著增强肿瘤治疗效果。2’3’-cGAMP与STING结合后,STING需要从内质网经由高尔基体在核周囊泡聚集并招募、活化TBK1,即所谓STING的转运。参与STING转运的调控蛋白有不少重要发现,如武汉大学舒红兵教授发现iRhom2对STING转运及功能必不可少。但为什么STING活化必需从内质网转位至高尔基体一直是领域内悬而未决的重要科学问题。已有的研究表明STING的转位和激活紧密偶联:阻断膜泡运输的抑制剂BFA可完全阻断STING的激活,而STING的自激活突变体则会自发的定位于高尔基体。更加有趣的发现来源于最近关于COPA综合征的自身免疫疾病的研究。COPA是负责蛋白从高尔基体向内质网回收的COPI复合体的关键亚基,其突变会导致逃逸到高尔基体的STING无法向内质网回收,从而使STING在高尔基体累积并自激活,引发自身免疫疾病。携带COPA突变的细胞中STING的活化完全不依赖于cGAMP,说明定位于高尔基体的STING可自发活化,进而提示高尔基体中可能存在使STING活化的未知配体。
细胞间存在由细胞分泌的蛋白质和多糖构成的细胞外基质。胞外基质不仅为细胞提供支架,还对细胞存活、发育、迁移、增殖等有重要调控作用。粘多糖是一类在高尔基体合成的、由二糖重复单元构成的直链线性聚合物,其主要成分硫酸化糖胺聚糖(sulfated glycosaminoglycans,sGAGs)是胞外基质的重要成员,也是骨基质和结缔组织的主要成分。基于二糖单元的不同组成,可将硫酸化糖胺聚糖分为四大类:①硫酸皮肤素(dermatin sulfate,DS);②硫酸软骨素(chondroitin sulfate,CS);③硫酸角质素(keratan sulfate,KS);④硫酸类肝素(heparan sulfate,HS)和肝素(heparin,Hp)。硫酸化糖胺聚糖广泛分布于细胞外基质,细胞表面或胞内膜泡(高尔基体、内体及分泌小泡)。由于荷载大量带负电的硫酸化修饰,细胞外硫酸化糖胺聚糖和靶蛋白上正电或极性氨基酸残基结合,影响受体蛋白与其配体的相互作用或诱导受体寡聚,也被认为是一些膜受体的共配体。近年来的研究发现粘多糖具有抗凝血、降血脂、抗病毒、抗肿瘤及抗放射等多种药理活性作用。此外,粘多糖是动物药的活性成分之一,常见于皮(阿胶、海参、蝉蜕、蛇蜕等),骨(虎骨、狗骨等),角(犀角、鹿茸等),鳞甲(穿山甲、龟板、鳖甲、玳瑁等)及粘液(蜗牛、泥鳅等)等药材中,这些药材是我国数千年传统医药文化的瑰宝。已有的研究表明胞外硫酸化糖胺聚糖在调控很多种生理学功能方面发挥重要的作用,但胞内硫酸化糖胺聚糖的生理学功能知之甚少,它们参与天然免疫反应的功能从未见报道。
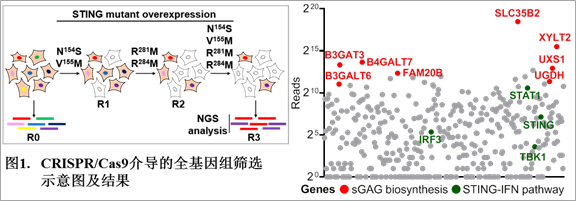
2021年4月14日,新葡萄8883官网AMG蒋争凡实验室在《Immunity》上以research
article形式在线发表了STING为什么需要进行高尔基体转运的机制研究“Golgi-synthesized
sulfated glycosaminoglycans
mediate polymerization and activation of the cGAMP sensor STING”,报道了高尔基体内合成的硫酸化糖胺聚糖作为STING共配体介导STING在高尔基体的活化。在本研究中,蒋争凡实验室的方润博士和蒋启飞同学巧妙地利用了STING自激活突变体诱导细胞死亡的特性,在二倍体细胞HT1080中进行了基于CRISPR–Cas9介导的全基因组筛选,发现多个参与硫酸化糖胺聚糖合成的关键基因被高度富集(图1)。这些粘多糖合成关键基因的敲除使细胞丧失了对STING的反应性。随后,他们通过在不同细胞中构建基因敲除细胞株,进一步证明在高尔基体内发生的硫酸化糖胺聚糖缺失会严重削弱cGAS-STING通路的激活。为了研究硫酸化糖胺聚糖是否直接作用于STING,他们选用了荷载硫酸化糖胺聚糖的核心蛋白SRGN作为硫酸化糖胺聚糖的指针,发现STING和SRGN存在DNA病毒诱导的共定位和相互作用(图2A)。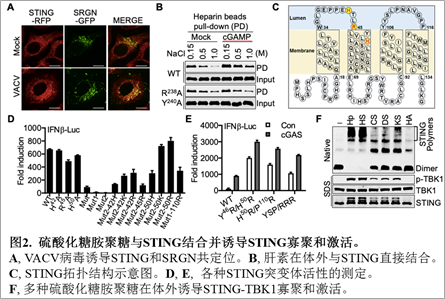 用携带肝素的磁珠进行体外pull-down实验也表明STING和肝素存在直接的相互作用,且结合cGAMP的STING具有更强的肝素结合能力(图2B)。硫酸化糖胺聚糖由于荷载大量带负电的硫酸化修饰,因而主要通过静电相互作用与靶蛋白上的正电氨基酸残基结合来发挥功能。由于胞内硫酸化糖胺聚糖存在于高尔基体腔内,他们推测位于STING第一和第二跨膜区之间的三个正电氨基酸残基(H42,R45,H50)可能参与结合硫酸化糖胺聚糖(图2C)。将这三个正电氨基酸进行突变会显著削弱STING的激活(图2D)。进一步将位于STING第一和第二跨膜区及第三和第四跨膜区内的极性氨基酸进行突变则会使STING的活性逐步降低直至完全消失。有意思的是,回复上述三个正电氨基酸中的任意一个都可使完全没有活性的突变体恢复部分功能。将42位或50位回复为电性更强的赖氨酸或精氨酸,STING的活性会随着回复的氨基酸的正电荷增多而逐渐增强。有意思的是,在不含有正电氨基酸的第三和第四跨膜区引入正电氨基酸(P110R)也会部分回复突变STING的活性。免疫共沉淀实验发现各种STING突变体与SRGN的相互作用强度和这些突变体的活性有非常一致的相关性;更重要的是,通过引入额外的带正电的精氨酸(Y46R/H50R,H50R/P110R等)则会使STING组成性地结合硫酸化糖胺聚糖而发生自激活(图2E)。这些结果表明硫酸化糖胺聚糖和STING的结合能力是决定STING能否激活及激活强度的决定因素之一。
用携带肝素的磁珠进行体外pull-down实验也表明STING和肝素存在直接的相互作用,且结合cGAMP的STING具有更强的肝素结合能力(图2B)。硫酸化糖胺聚糖由于荷载大量带负电的硫酸化修饰,因而主要通过静电相互作用与靶蛋白上的正电氨基酸残基结合来发挥功能。由于胞内硫酸化糖胺聚糖存在于高尔基体腔内,他们推测位于STING第一和第二跨膜区之间的三个正电氨基酸残基(H42,R45,H50)可能参与结合硫酸化糖胺聚糖(图2C)。将这三个正电氨基酸进行突变会显著削弱STING的激活(图2D)。进一步将位于STING第一和第二跨膜区及第三和第四跨膜区内的极性氨基酸进行突变则会使STING的活性逐步降低直至完全消失。有意思的是,回复上述三个正电氨基酸中的任意一个都可使完全没有活性的突变体恢复部分功能。将42位或50位回复为电性更强的赖氨酸或精氨酸,STING的活性会随着回复的氨基酸的正电荷增多而逐渐增强。有意思的是,在不含有正电氨基酸的第三和第四跨膜区引入正电氨基酸(P110R)也会部分回复突变STING的活性。免疫共沉淀实验发现各种STING突变体与SRGN的相互作用强度和这些突变体的活性有非常一致的相关性;更重要的是,通过引入额外的带正电的精氨酸(Y46R/H50R,H50R/P110R等)则会使STING组成性地结合硫酸化糖胺聚糖而发生自激活(图2E)。这些结果表明硫酸化糖胺聚糖和STING的结合能力是决定STING能否激活及激活强度的决定因素之一。
为了进一步研究硫酸化糖胺聚糖如何介导STING的激活,他们通过体外实验发现多种硫酸化糖胺聚糖可不同程度地诱导STING全长蛋白发生多聚体化并诱导激酶TBK1的活化,其中硫酸肝素(HS)和肝素(Hp)的激活效果最佳(图2E)。进一步实验发现硫酸化糖胺聚糖激活STING是糖链长度依赖的,最短由四个单糖形成的糖链即具有激活STING的能力,并且这种激活依赖于糖链上的O-位硫酸化修饰。更为重要的是,通过对人、小鼠、蝙蝠和鸡四种来源的STING进行分析发现,硫酸化糖胺聚糖介导STING激活的机制在进化上是高度保守的。最后,他们通过小鼠实验表明硫酸化糖胺聚糖的合成对于小鼠抵抗DNA病毒感染十分关键。
综上所述,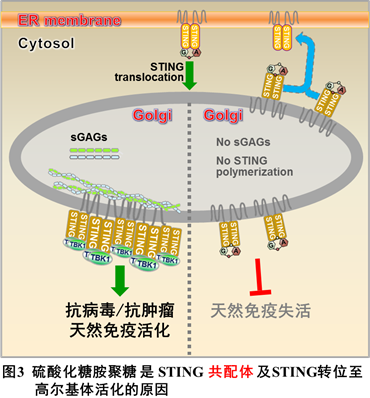 该研究发现:1)STING活化需要两种配体。第一种配体是环化二核苷酸(其中2’3’-cGAMP结合能力最强),与STING细胞质一侧的环化二核苷酸结合区域结合并导致STING转位至高尔基体;第二种配体为本研究发现的高尔基体内sGAGs,与STING高尔基体内一侧的正电荷(极性)氨基酸结合,像铰链一样引发STING多聚化,进而招募并促进TBK1自磷酸化及下游通路活化(图3)。2)揭开了“为什么STING必需去高尔基体活化”这一重要的科学谜题,有望打通STING活化的“最后一公里”。3)填补了胞内硫酸化糖胺聚糖的生理学功能研究空白,揭示了生物多糖在细胞内的关键免疫学功能,为未来生物多糖在抗病毒、抗肿瘤的临床实践提供新的线索。
该研究发现:1)STING活化需要两种配体。第一种配体是环化二核苷酸(其中2’3’-cGAMP结合能力最强),与STING细胞质一侧的环化二核苷酸结合区域结合并导致STING转位至高尔基体;第二种配体为本研究发现的高尔基体内sGAGs,与STING高尔基体内一侧的正电荷(极性)氨基酸结合,像铰链一样引发STING多聚化,进而招募并促进TBK1自磷酸化及下游通路活化(图3)。2)揭开了“为什么STING必需去高尔基体活化”这一重要的科学谜题,有望打通STING活化的“最后一公里”。3)填补了胞内硫酸化糖胺聚糖的生理学功能研究空白,揭示了生物多糖在细胞内的关键免疫学功能,为未来生物多糖在抗病毒、抗肿瘤的临床实践提供新的线索。
北京大学生科院博士后方润和2015级博士生蒋启飞为该文章的共同第一作者,生科院/北大-清华生命科学联合中心的蒋争凡教授为通讯作者。本研究工作得到了国家自然科学基金委、科技部国家重点基础研究项目、北京大学“细胞增殖与分化”教育部重点实验室及“北大-清华生命科学联合中心”的资助。
原文链接:https://www.cell.com/immunity/fulltext/S1074-7613(21)00123-0