检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
/ 老版新葡萄8883官网 / 学术科研
2016年5月23日,新葡萄8883官网AMG生物动态光学成像中心孙育杰研究组与清华大学生命学院俞立研究组合作在《Developmental Cell》发表论文《Kinesin 1drives autolysosome tubulation》(驱动蛋白介导自噬性溶酶体出管),文章通过在体外重构自噬性溶酶体出管的单分子研究体系详细解析了驱动蛋白KIF5B介导自噬性溶酶体出管再生的分子机制。研究发现网格蛋白调控自噬溶酶体膜上PtdIns(4,5)P2聚集成微区,KIF5B通过与PtdIns(4,5)P2的直接相互作用而被招募到PtdIns(4,5)P2微区处,随后通过KIF5B的驱动蛋白性质,拉动了自噬溶酶体管状结构的生成。此项研究成果可能揭示了一个生物膜系统中普遍存在的由驱动蛋白介导的膜形变机制。
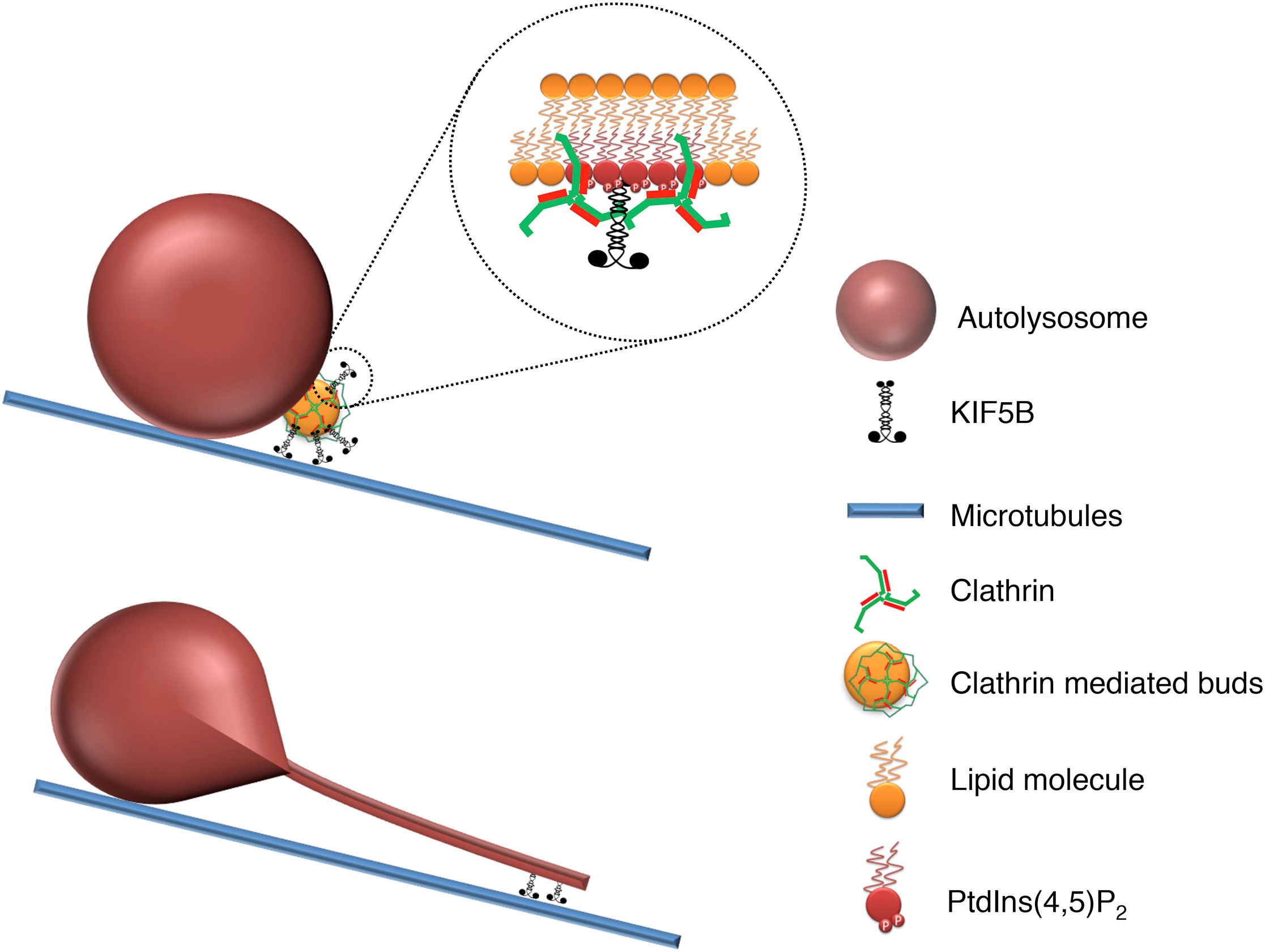
单分子体外重构体系解析马达蛋白驱动的生物膜形变分子机制
从2011年起,孙育杰研究组与俞立研究组合作建立单分子体外重构实验体系,结合细胞生物学研究方法研究生物膜形变的分子生物学机制和物理机制,5年的合作硕果丰厚。于2015年在《Cell Research》发表文章,揭示一种新的线粒体动态行为“线粒体动态管化”,是线粒体形成网络的重要补充机制,并体外重构了该过程。被选为《Cell Research》10月刊的封面文章。于2016年初在《Scientific report》发表文章,利用体外重构实验和超高分辨率显微镜技术,揭示细胞内囊泡的体积是调控生物膜形变,例如出管的重要决定因素之一。上文所述发表在《Developmental Cell》的文章是合作发表的第三篇论文。
原文链接:http://www.cell.com/developmental-cell/fulltext/S1534-5807%2816%2930234-9