检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
/ 老版新葡萄8883官网 / 学术科研
2021年10月9日,生科院蒋争凡实验室和西北农林科大沈锡辉实验室与军事医学院周冬生实验室合作在国际著名学术期刊《PNAS》上以Research Article形式在线发表了他们在抗细菌天然免疫研究领域的最新成果----T6SS translocates a micropeptide to suppress STING-mediated innate immunity by sequestering manganese。
天然免疫通过模式识别受体感知病原体入侵,激活下游反应抵抗病原体感染。STING(MITA/ERIS)是细胞质内环化二核苷酸(CDN,包括细菌特有的c-di-GMP, c-di-AMP及多种连接方式的cGAMPs)受体。CDN与STING在细胞质一侧结合并导致STING转位至高尔基体;而高尔基体内合成的硫酸化糖胺聚糖(sGAGs)与STING高尔基体内一侧的氨基酸结合并引发STING多聚化,招募激酶TBK1,最终诱导I-型干扰素等细胞因子产生。自1987年在木醋杆菌(A. xylinum)发现c-di-GMP,2008年在枯草芽孢杆菌(B. subtilis)发现c-di-AMP及2012年在霍乱弧菌(V. cholerae)发现3’3’-cGAMP以来,已知绝大多数细菌都产生这些对其增殖、分化及侵染至关重要的第二信使。作为重要的防御手段,宿主细胞则产生了能够特异性识别这些对细菌不可或缺产物的受体(此处为STING蛋白),并激活宿主的抗细菌天然免疫反应。
细菌六型分泌系统(T6SS, type VI secretion system)是当前微生物领域的研究热点之一,可将多种效应蛋白投递至胞外环境、其它细菌或者宿主细胞内,在细菌抗胁迫、菌间竞争及与宿主的相互作用中发挥重要作用。2017年,沈锡辉实验室发现泰国伯克霍尔德氏菌(B. thailandensis)T6SS通过分泌一个锰离子结合效应蛋白TseM介导锰离子的运输,促进细菌的抗氧化胁迫能力和致病性。2018年蒋争凡实验室则揭示病毒感染导致宿主细胞内不同细胞器释放锰离子强烈促进cGAS-STING通路激活抵抗病毒感染。这些发现促使他们进一步探究这类具有锰离子结合功能的T6SS效应蛋白能否通过影响宿主胞内的锰离子水平来调节宿主天然免疫。
本研究发现革兰氏阴性菌假结核耶尔森氏菌(Y. pseudotuberculosis,Yptb)T6SS可分泌一个仅由48个氨基酸组成的锰离子结合蛋白TssS(T6SS-secreted micropeptide suppressing STING)促进细菌对锰离子的摄取。该基因缺失的突变体菌株(ΔtssS)对小鼠致病性显著下降,感染ΔtssS菌株小鼠的不同组织器官内细菌载量也明显下降。转录组学分析发现,与感染野生型菌株相比,感染ΔtssS菌株细胞内的I-型干扰素(Type I-IFNs)及干扰素刺激基因(IFN-stimulated genes, ISGs)表达明显上升,提示TssS能够抑制宿主抗细菌天然免疫反应;而将TssS中锰离子结合位点突变后,其对天然免疫系统的抑制能力和对小鼠的致病性显著下降,说明TssS的锰离子结合能力对其抑制天然免疫至关重要。进一步研究发现 LPS(革兰氏阴性菌细胞壁组分)处理能显著升高细胞质锰离子浓度,但在细胞中过表达TssS蛋白则能够抑制cGAMP/c-di-GMP所诱导的STING活化和下游基因表达。假结核耶尔森氏菌(Yptb)及同属的鼠疫杆菌(Y. pestis)和小肠结肠炎耶尔森菌(Y. enterocolitica)都产生对其存活、侵染非常重要的c-di-GMP。以往的研究表明锰离子可显著促进c-di-GMP与STING的结合。与此相一致,野生型Yptb或ΔtssS突变体感染野生型小鼠后,Yptb野生型感染的小鼠中细菌载量显著高于ΔtssS感染小鼠;而当这两种菌株分别感染STING缺失小鼠时,不同感染组之间细菌载量的巨大差异显著缩小。这些结果表明:一方面细菌产物LPS和c-di-GMP分别诱导宿主细胞内锰离子释放并共同促进STING活化;另一方面细菌产生并分泌TssS通过螯合胞内锰离子以削弱c-di-GMP对STING的结合及激活能力,实现对宿主抗细菌天然免疫反应的抑制。
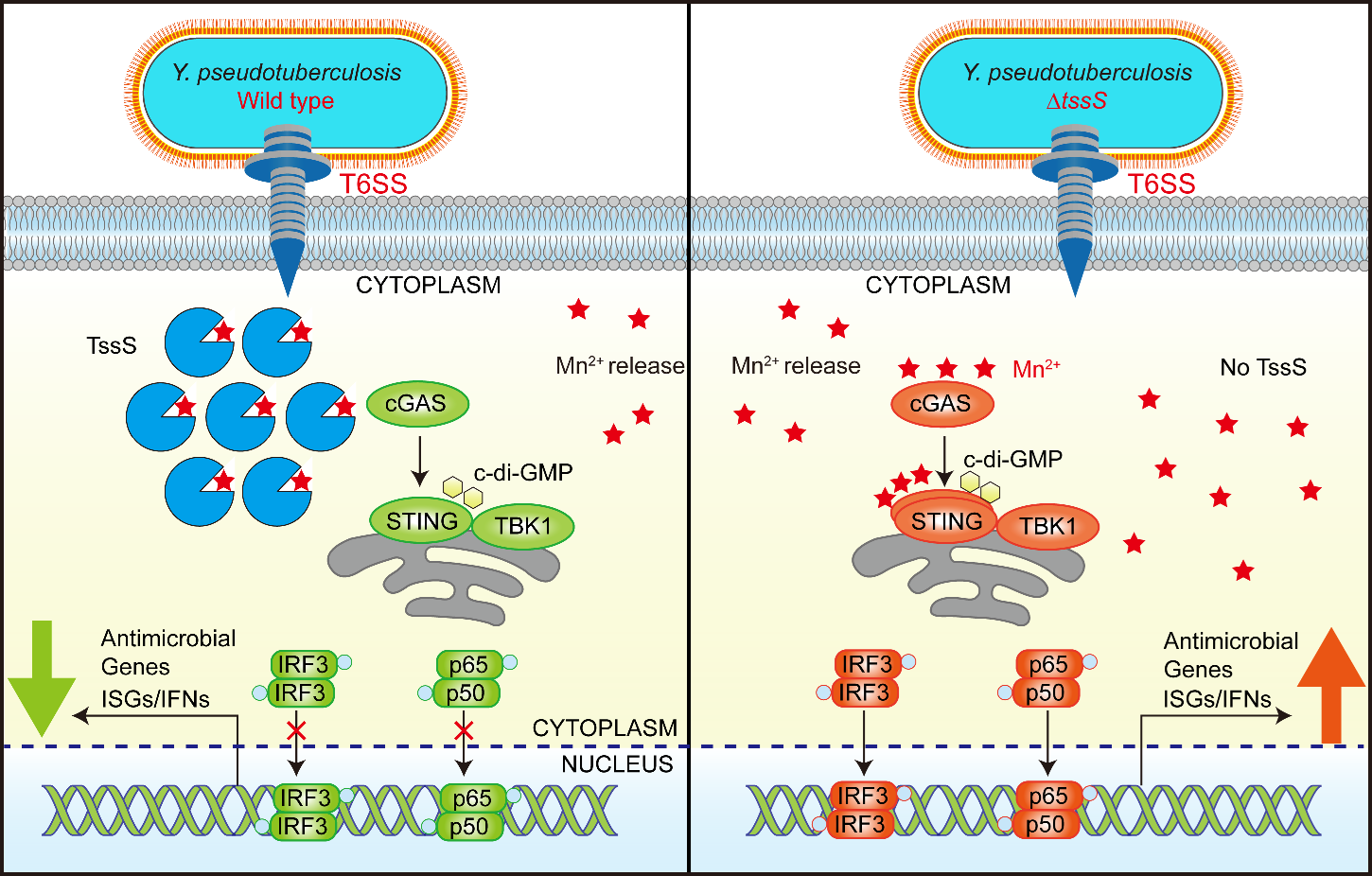
TssS螯合锰离子抑制宿主细胞内STING介导的抗细菌天然免疫反应
与其它已知细菌效应蛋白通常通过与宿主胞内蛋白、核酸等大分子相互作用以致病的方式不同,本研究揭示了一个细菌效应蛋白通过螯合宿主细胞内锰离子,从而抑制宿主天然免疫反应的新机制(如图所示)。作为一种新的细菌免疫逃逸机制,该研究为理解T6SS在细菌致病机制中的作用提供了新的视角,不仅对于深入理解病原微生物调节宿主免疫反应的分子机制有重要意义,也将为治疗一些自身免疫系统过度激活引起的疾病提供新的思路。更重要的是,在大量不同种属细菌的T6SS基因簇中都鉴定到类似功能未知的Mn2+结合蛋白,暗示本研究发现的天然免疫逃逸机制是一个细菌中普遍存在的、古老的抗宿主反应机制。
西北农林科大博士后朱玲芳、徐磊和北大生科院博士后王晨光为本论文共同第一作者,沈锡辉、蒋争凡和周冬生为共同通讯作者。本研究得到了“北大-清华生命科学联合中心”、北京大学“细胞增殖与分化”教育部重点实验室、国家重点研发计划、国家自然科学基金、中国博士后科学基金及西北农林科技大学双一流学科群建设计划等项目的资助。